Atualmente, a doença hepática gordurosa não alcoólica (DHGNA) tornou-se a principal causa de doença hepática crônica na China e até mesmo no mundo. O espectro da doença inclui esteato-hepatite hepática simples, esteato-hepatite não alcoólica (EHNA) e cirrose e câncer de fígado relacionados. A EHNA é caracterizada pelo acúmulo excessivo de gordura nos hepatócitos e induz dano celular e inflamação, com ou sem fibrose hepática. A gravidade da fibrose hepática em pacientes com EHNA está intimamente associada a mau prognóstico hepático (cirrose e suas complicações e carcinoma hepatocelular), eventos cardiovasculares, malignidades extra-hepáticas e morte por todas as causas. A EHNA pode afetar negativamente a qualidade de vida dos pacientes; no entanto, nenhum medicamento ou terapia foi aprovado para tratar a EHNA.
Um estudo recente (ENLIVEN) publicado no New England Journal of Medicine (NEJM) mostrou que a pegozafermina melhorou tanto a fibrose hepática quanto a inflamação hepática em pacientes com NASH não cirróticos confirmados por biópsia.
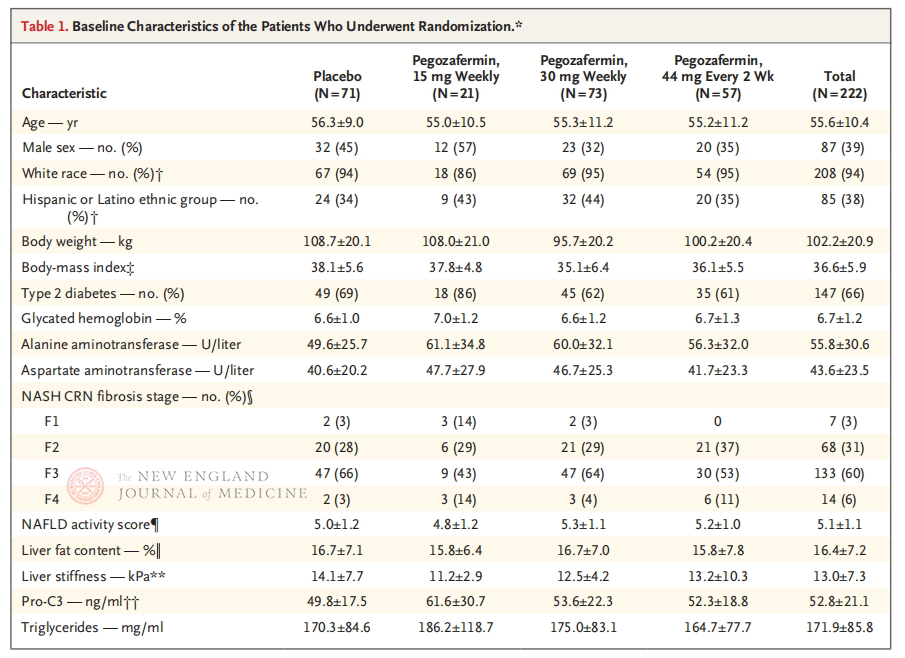
O ensaio clínico multicêntrico, randomizado, duplo-cego e controlado por placebo de Fase 2b, conduzido pelo Professor Rohit Loomba e sua equipe clínica na Faculdade de Medicina da Universidade da Califórnia, San Diego, incluiu 222 pacientes com NASH estágio F2-3 confirmado por biópsia entre 28 de setembro de 2021 e 15 de agosto de 2022. Eles foram aleatoriamente designados para receber pegozafermina (injeção subcutânea, 15 mg ou 30 mg uma vez por semana, ou 44 mg uma vez a cada 2 semanas) ou placebo (uma vez por semana ou uma vez a cada 2 semanas). Os desfechos primários incluíram melhora ≥ estágio 1 na fibrose e nenhuma progressão da NASH. A NASH foi resolvida sem progressão fibrótica. O estudo também conduziu uma avaliação de segurança.
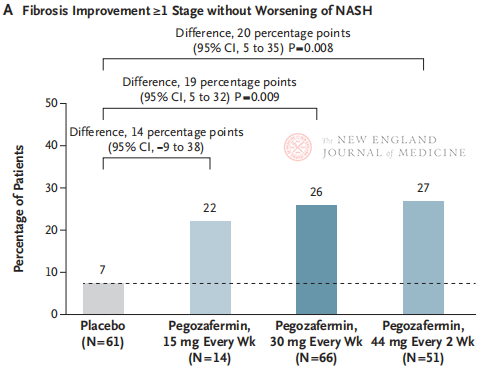
Após 24 semanas de tratamento, a proporção de pacientes com melhora ≥ estágio 1 na fibrose e sem piora da NASH, e a proporção de pacientes com regressão da NASH e sem piora da fibrose foram significativamente maiores nos três grupos de dose de Pegozafermina do que no grupo placebo, com diferenças mais significativas em pacientes tratados com 44 mg uma vez a cada duas semanas ou 30 mg uma vez por semana. Em termos de segurança, a pegozafermina foi semelhante ao placebo. Os eventos adversos mais comuns associados ao tratamento com pegozafermina foram náusea, diarreia e eritema no local da injeção. Neste estudo de fase 2b, os resultados preliminares sugerem que o tratamento com pegozafermina melhora a fibrose hepática.
A pegozafermina, utilizada neste estudo, é um análogo glicolado de ação prolongada do fator de crescimento de fibroblastos humano 21 (FGF21). O FGF21 é um hormônio metabólico endógeno secretado pelo fígado, que desempenha um papel na regulação do metabolismo de lipídios e glicose. Estudos anteriores demonstraram que o FGF21 tem efeitos terapêuticos em pacientes com NASH, aumentando a sensibilidade hepática à insulina, estimulando a oxidação de ácidos graxos e inibindo a lipogênese. No entanto, a curta meia-vida do FGF21 natural (cerca de 2 horas) limita seu uso no tratamento clínico da NASH. A pegozafermina utiliza a tecnologia de peguilação glicosilada para estender a meia-vida do FGF21 natural e otimizar sua atividade biológica.
Além dos resultados positivos neste ensaio clínico de Fase 2b, outro estudo recente publicado na Nature Medicine (ENTRIGUE) mostrou que a pegozafermina também reduziu significativamente os triglicerídeos, o colesterol não HDL, a apolipoproteína B e a esteatose hepática em pacientes com hipertrigliceridemia grave, o que pode ter um impacto positivo na redução do risco de eventos cardiovasculares em pacientes com NASH.
Esses estudos sugerem que a pegozafermina, como um hormônio metabólico endógeno, pode proporcionar múltiplos benefícios metabólicos a pacientes com NASH, especialmente porque a NASH poderá ser renomeada para doença hepática gordurosa associada ao metabolismo no futuro. Esses resultados a tornam um medicamento potencial muito importante para o tratamento da NASH. Ao mesmo tempo, esses resultados positivos do estudo apoiarão a pegozafermina em ensaios clínicos de fase 3.
Embora tanto o tratamento quinzenal com 44 mg quanto o tratamento semanal com 30 mg de pegozafermina tenham atingido o desfecho primário histológico do estudo, a duração do tratamento neste estudo foi de apenas 24 semanas, e a taxa de adesão no grupo placebo foi de apenas 7%, significativamente menor do que os resultados de estudos clínicos anteriores com duração de 48 semanas. As diferenças e a segurança são as mesmas? Dada a heterogeneidade da EHNA, ensaios clínicos internacionais, multicêntricos e maiores são necessários no futuro para incluir populações maiores de pacientes e estender a duração do tratamento para melhor avaliar a eficácia e a segurança do medicamento.
Horário da postagem: 16 de setembro de 2023