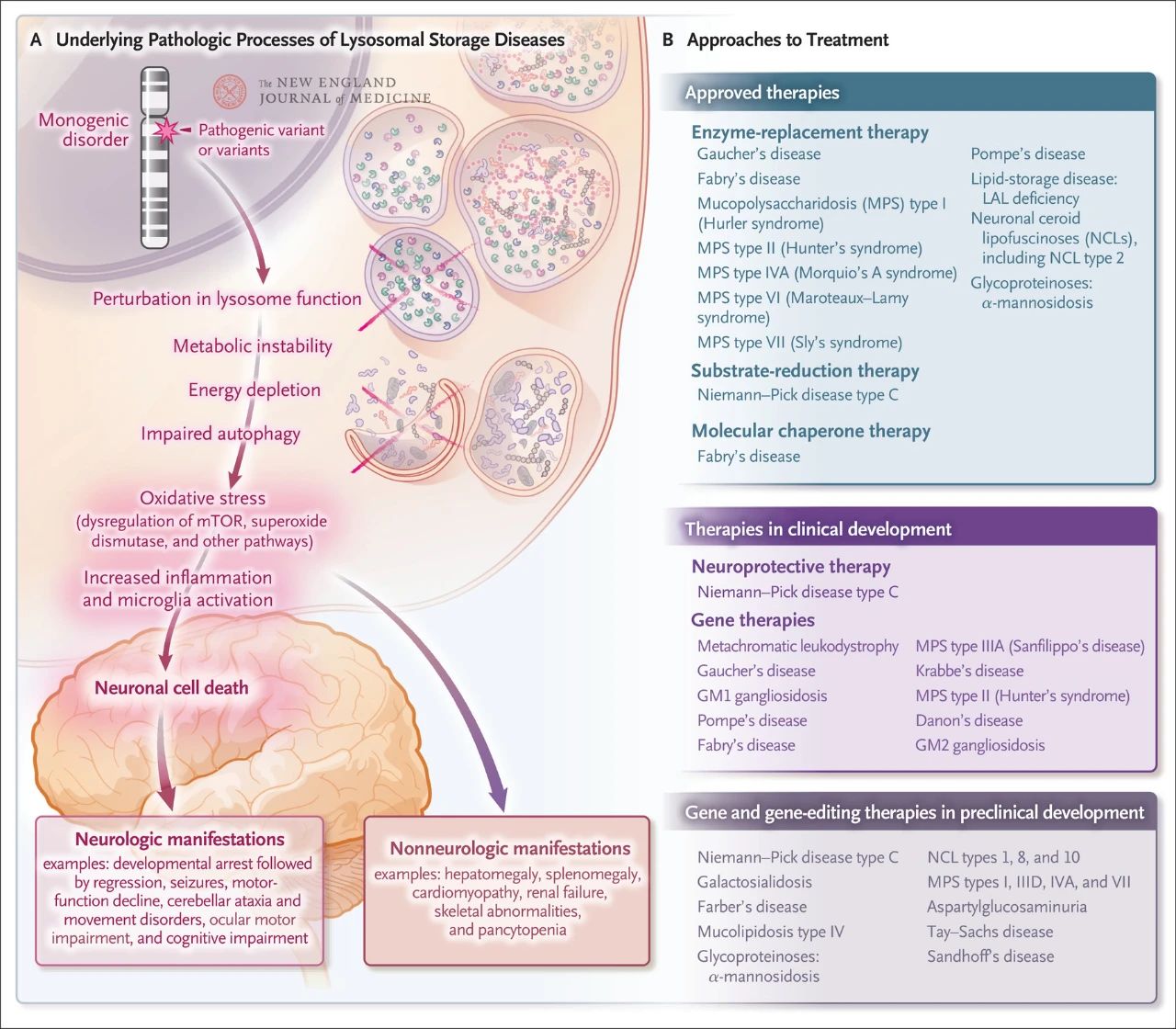
Embora relativamente rara, a incidência geral de armazenamento lisossomal é de cerca de 1 em cada 5.000 nascidos vivos. Além disso, dos quase 70 distúrbios de armazenamento lisossomal conhecidos, 70% afetam o sistema nervoso central. Esses distúrbios de gene único causam disfunção lisossomal, resultando em instabilidade metabólica, desregulação da proteína-alvo da rapamicina em mamíferos (mTOR, que normalmente inibe a inflamação), comprometimento da autofagia e morte de células nervosas. Diversas terapias que visam os mecanismos patológicos subjacentes à doença de armazenamento lisossomal foram aprovadas ou estão em desenvolvimento, incluindo terapia de reposição enzimática, terapia de redução de substrato, terapia com chaperonas moleculares, terapia gênica, edição gênica e terapia neuroprotetora.
A doença de Niemann-Pick tipo C é um distúrbio lisossomal do transporte de colesterol celular causado por mutações bialélicas no gene NPC1 (95%) ou NPC2 (5%). Os sintomas da doença de Niemann-Pick tipo C incluem declínio neurológico rápido e fatal na infância, enquanto as formas de início tardio, juvenil e adulto incluem esplenomegalia, paralisia supranuclear do olhar e ataxia cerebelar, disarticulação e demência progressiva.
Nesta edição do periódico, Bremova-Ertl et al. relatam os resultados de um ensaio clínico duplo-cego, controlado por placebo e cruzado. O ensaio utilizou um potencial agente neuroprotetor, o análogo de aminoácido N-acetil-L-leucina (NALL), para tratar a doença de Niemann-Pick tipo C. Foram recrutados 60 pacientes adolescentes e adultos sintomáticos, e os resultados mostraram melhora significativa na pontuação total (desfecho primário) da Escala de Avaliação e Classificação da Ataxia.
Os ensaios clínicos com N-acetil-DL-leucina (Tanganil), um racêmico de NALL e n-acetil-D-leucina, parecem ser amplamente orientados pela experiência: o mecanismo de ação não foi claramente elucidado. A N-acetil-dl-leucina foi aprovada para o tratamento da vertigem aguda desde a década de 1950; modelos animais sugerem que o medicamento atua reequilibrando a superpolarização e a despolarização dos neurônios vestibulares mediais. Posteriormente, Strupp et al. relataram os resultados de um estudo de curto prazo no qual observaram melhoras nos sintomas em 13 pacientes com ataxia cerebelar degenerativa de diversas etiologias, descobertas que reacenderam o interesse em analisar o medicamento novamente.
O mecanismo pelo qual a n-acetil-DL-leucina melhora a função nervosa ainda não está claro, mas os achados em dois modelos murinos, um de doença de Niemann-Pick tipo C e outro de distúrbio de depósito gangliosídeo GM2 variante O (doença de Sandhoff), outra doença lisossomal neurodegenerativa, levaram a atenção para a LNA. Especificamente, a sobrevivência de camundongos Npc1-/- tratados com n-acetil-DL-leucina ou LNA (enantiômeros L) melhorou, enquanto a sobrevivência de camundongos tratados com n-acetil-D-leucina (enantiômeros D) não melhorou, sugerindo que a LNA é a forma ativa do fármaco. Em um estudo semelhante sobre a variante O do distúrbio de depósito gangliosídeo GM2 (Hexb-/-), a n-acetil-DL-leucina resultou em uma extensão modesta, mas significativa, da expectativa de vida em camundongos.
Para explorar o mecanismo de ação da n-acetil-DL-leucina, os pesquisadores investigaram a via metabólica da leucina medindo metabólitos nos tecidos cerebelares dos animais mutantes. Em um modelo variante O do distúrbio de armazenamento gangliosídeo GM2, a n-acetil-DL-leucina normaliza o metabolismo da glicose e do glutamato, aumenta a autofagia e aumenta os níveis de superóxido dismutase (um sequestrador ativo de oxigênio). No modelo C da doença de Niemann-Pick, foram observadas alterações no metabolismo da glicose e dos antioxidantes, além de melhorias no metabolismo energético mitocondrial. Embora a L-leucina seja um potente ativador de mTOR, não houve alteração no nível ou na fosforilação de mTOR após o tratamento com n-acetil-DL-leucina ou seus enantiômeros em nenhum dos modelos murinos.
O efeito neuroprotetor da NALL foi observado em um modelo murino de lesão cerebral induzida por impacto cortical. Esses efeitos incluem a redução de marcadores neuroinflamatórios, a redução da morte celular cortical e a melhora do fluxo de autofagia. Após o tratamento com NALL, as funções motoras e cognitivas dos camundongos lesionados foram restauradas e o tamanho da lesão foi reduzido.
A resposta inflamatória do sistema nervoso central é a marca registrada da maioria dos distúrbios neurodegenerativos de depósito lisossomal. Se a neuroinflamação puder ser reduzida com o tratamento da LNA, os sintomas clínicos de muitos, se não todos, os distúrbios neurodegenerativos de depósito lisossomal podem ser melhorados. Como este estudo demonstra, espera-se que a LNA também tenha sinergias com outras terapias para a doença de depósito lisossomal.
Muitos distúrbios de armazenamento lisossomal também estão associados à ataxia cerebelar. De acordo com um estudo internacional envolvendo crianças e adultos com distúrbios de armazenamento de gangliosídeos GM2 (doença de Tay-Sachs e doença de Sandhoff), a ataxia foi reduzida e a coordenação motora fina melhorou após o tratamento com NALL. No entanto, um grande estudo multicêntrico, duplo-cego, randomizado e controlado por placebo mostrou que a n-acetil-DL-leucina não foi clinicamente eficaz em pacientes com ataxia cerebelar mista (hereditária, não hereditária e inexplicada). Essa descoberta sugere que a eficácia pode ser observada apenas em estudos envolvendo pacientes com ataxia cerebelar hereditária e os mecanismos de ação associados analisados. Além disso, como a NALL reduz a neuroinflamação, que pode levar a lesão cerebral traumática, estudos com NALL para o tratamento de lesão cerebral traumática podem ser considerados.
Horário da postagem: Mar-02-2024