A hiperlipidemia mista é caracterizada por níveis plasmáticos elevados de lipoproteínas de baixa densidade (LDL) e lipoproteínas ricas em triglicerídeos, levando a um risco aumentado de doença cardiovascular aterosclerótica nessa população de pacientes.
ANGPTL3 inibe a lipase lipoproteica e a endosepiase, bem como a captação hepática de lipoproteínas ricas em triglicerídeos. Portadores da variante inativada de ANGPTL3 apresentaram níveis mais baixos de triglicerídeos, colesterol LDL, colesterol de lipoproteína de alta densidade (HDL) e colesterol não HDL, além de menor risco de doença cardiovascular aterosclerótica. Zodasiran é um fármaco de RNA interferente pequeno (RNAi) que tem como alvo a expressão de ANGPTL3 no fígado.
Hiperlipidemia mista refere-se a níveis elevados de colesterol de lipoproteína de baixa densidade (LDL-C) e lipoproteínas ricas em triglicerídeos. As lipoproteínas ricas em triglicerídeos (incluindo quilomícrons, lipoproteínas de densidade muito baixa (VLDL) e colesterol residual) desempenham um papel importante no desenvolvimento da doença aterosclerótica. Não há tratamento eficaz para a hiperlipidemia mista.
Sabe-se que os Bates reduzem os níveis de triglicerídeos (TG), mas essa redução é limitada. Ao mesmo tempo, medicamentos redutores de TG, incluindo Bates (como ácido acético eicosapentaenoico, etc.), não têm efeito significativo sobre o risco de doença aterosclerótica causada por níveis elevados de colesterol residual. Além disso, estudos anteriores em pacientes que já tomavam estatinas demonstraram que a combinação de medicamentos redutores de TG não reduz o risco de eventos cardiovasculares. Esses fatores dificultam muito o tratamento da hiperlipidemia mista.
A ANGPTL3 (proteína 3 semelhante à angiopoietina) regula o metabolismo de lipídios e lipoproteínas, incluindo triglicerídeos e colesterol de lipoproteína de baixa densidade (HDL-C), inibindo reversivelmente a lipase lipoproteica, a endosepiase e a captação de lipoproteínas hepáticas dependentes do receptor de lipoproteína de baixa densidade (LDL). Descobriu-se que a variante de inativação da ANGPTL3 leva ao aumento da atividade da lipase lipoproteica e da endosepiase, o que, por sua vez, leva a baixos níveis plasmáticos de lipoproteínas na maioria dos casos. Isso inclui lipoproteínas ricas em triglicerídeos (ou seja, quilomícrons, colesterol residual, VLDL, lipoproteína de média densidade [IDL]), LDL, lipoproteína de alta densidade (HDL), lipoproteína (a) e seus componentes de colesterol. Pessoas heterozigotas portadoras dessa variante apresentam um risco reduzido de aproximadamente 40% de doença aterosclerótica, e nenhum fenótipo clínico adverso foi encontrado. ANGPTL3 é expresso no fígado, e terapias de silenciamento genético direcionadas ao seu mRNA, conhecidas como medicamentos de pequeno RNA interferente (siRNA), são um tratamento híbrido promissor para hiperlipidemia.
Em 12 de setembro de 2024, o New England Journal of Medicine (NEJM) publicou um estudo ARCHES 2 confirmando que o medicamento siRNA zodasiran reduziu significativamente os níveis de TG em pacientes com hiperlipidemia mista [1]. O ARCHES-2 é um estudo de fase 2b, duplo-cego, controlado por placebo, de exploração de intervalo de dose. Um total de 204 pacientes com hiperlipidemia mista (níveis de TG em jejum de 150-499 mg/dL, níveis de LDL-C ³70 mg/dL ou níveis de não-HDL-C ³100 mg/dL) foram incluídos. Eles foram divididos em grupo zodasiran 50 mg, grupo 100 mg, grupo 200 mg e grupo controle placebo. Os pacientes receberam injeções subcutâneas na semana 1 e 12 e receberam profilaxia de acompanhamento até a semana 36.
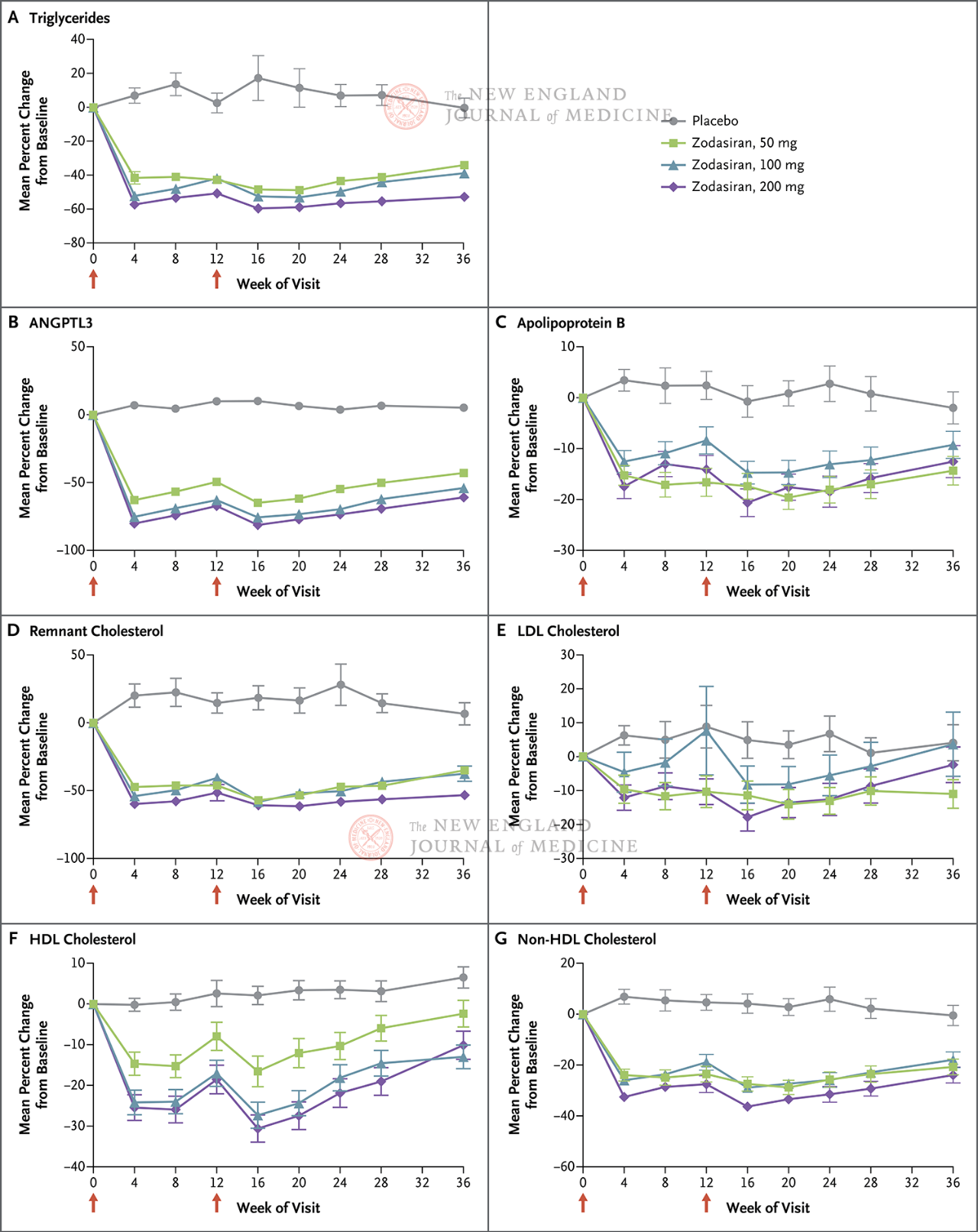
O desfecho primário foi a variação percentual nos TG da linha de base até a semana 24. O estudo constatou que, na semana 24, os níveis de TG no grupo zodasiran foram significativamente reduzidos de forma dose-dependente (os níveis de TG em cada grupo de dose foram reduzidos em 51, 57 e 63 pontos percentuais, respectivamente, em comparação com aqueles no grupo placebo) (P < 0,001 para todas as comparações). O ANGPTL3 também diminuiu em 54 pontos percentuais, 70 pontos percentuais e 74 pontos percentuais, respectivamente. Os níveis de colesterol não HDL diminuíram em 29 pontos percentuais, 29 pontos percentuais e 36 pontos percentuais, os níveis de apolipoproteína B diminuíram em 19 pontos percentuais, 15 pontos percentuais e 22 pontos percentuais, e os níveis de LDL-C diminuíram em 16 pontos percentuais, 14 pontos percentuais e 20 pontos percentuais, respectivamente, e esses resultados persistiram até a 36ª semana. Na semana 24, zodasiran
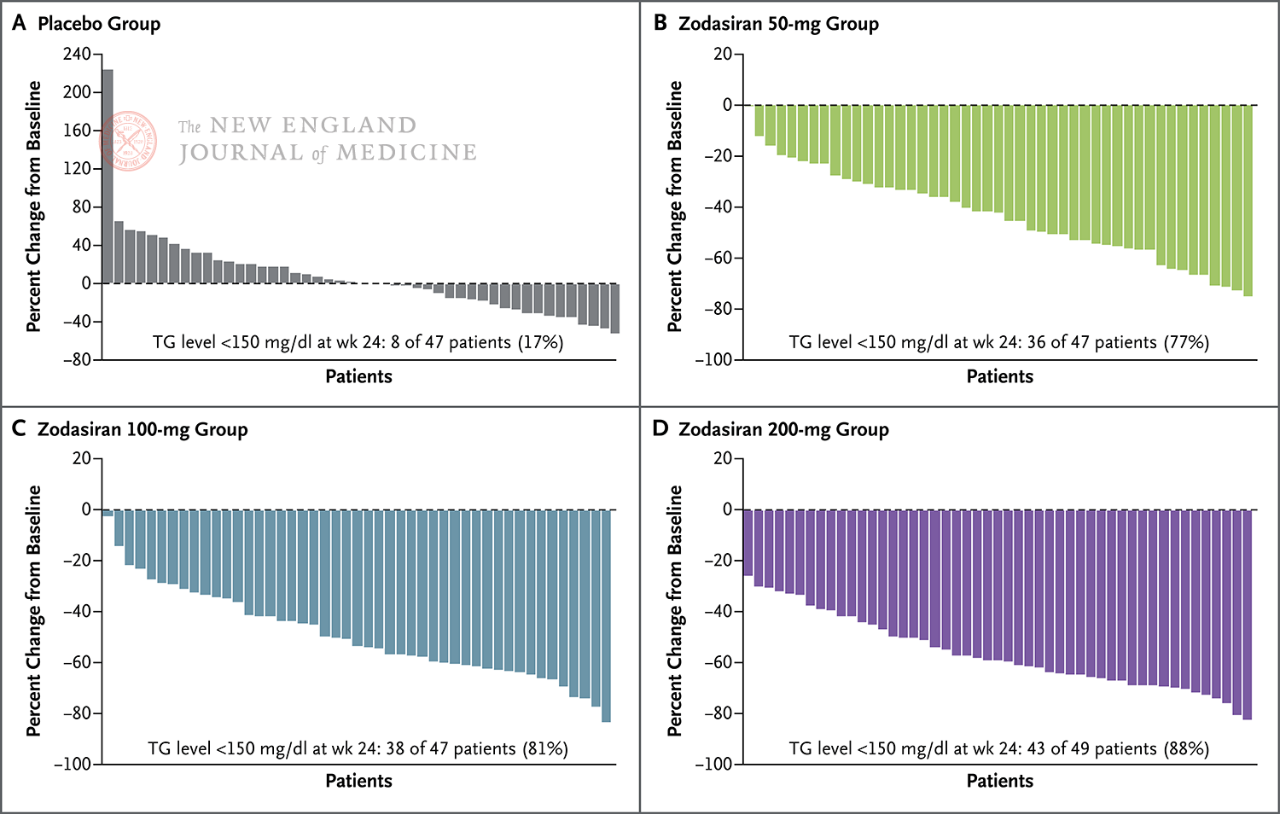
Em 88% dos pacientes no grupo de 200 mg, os TG em jejum caíram para a faixa normal.
As setas vermelhas nos dias 1 e 12 indicam administração de zodasiran ou placebo.
Os níveis de TG em jejum diminuíram para o normal na semana 24 (150
mg/dL ou menos)
Cada pilar representa um paciente.
O estudo também observou que o zotasiran foi seguro em todos os grupos de dosagem, com apenas 2 pacientes descontinuando o estudo devido a eventos adversos (1 no grupo placebo e 1 no grupo de 100 mg de zotasiran). Todos os eventos adversos graves no grupo zotasiran se recuperaram ao final do estudo, e houve uma morte no grupo placebo. O único evento adverso preocupante foi um aumento na HBA1c no grupo de 200 mg de zotasiran em comparação com o placebo (variação média da linha de base até a semana 24 [±DP], 0,38 ± 0,66% vs. -0,03 ± 0,88% em pacientes com diabetes preexistente). Pacientes sem diabetes foram 0,12 ± 0,19% vs. -0,03 ± 0,19%).
Em particular, quase todos os pacientes do estudo (96%) estavam sendo tratados com estatinas (37% das quais em altas doses), 1% estavam sendo tratados com um inibidor da enzima conversora de pró-proteína subtilisina 9 (PCSK9i) e 21% estavam sendo tratados com fibratos. Portanto, a adição de zodasirana ao regime de tratamento convencional atual ainda obteve efeitos hipolipemiantes consideráveis, o que proporciona um novo regime para o tratamento da hiperlipidemia mista no futuro.
Na semana 24, a dose máxima de 200 mg de zotasiran no estudo reduziu os níveis de colesterol residual em 34,4 mg/dL em comparação ao placebo. Com base nos modelos atuais, espera-se que essa redução reduza os principais eventos adversos cardíacos em 20%. O zotasiran tem potencial para ser usado como monoterapia para todos os componentes da lipoproteína, reduzindo o risco de eventos cardiovasculares em pacientes. Portanto, pesquisas adicionais são necessárias para determinar o potencial desse medicamento na redução do risco de doença aterosclerótica.
O estudo MUIR de Fase 2b, duplo-cego, randomizado e controlado por placebo, publicado simultaneamente no NEJM, utilizou outro medicamento siRNA, o plozasiran, para tratar hiperlipidemia mista [2]. O plozasiran foi desenvolvido para reduzir a expressão de APOC3, o gene que codifica a apolipoproteína C3 (APOC3), um regulador do metabolismo de TG, no fígado, reduzindo assim os níveis de TG e colesterol residual. As reduções nos níveis de TG e colesterol residual observadas no estudo foram semelhantes às encontradas no estudo ARCHES-2. Portanto, especula-se que, em pacientes com hiperlipidemia mista, os dois medicamentos tenham efeitos semelhantes na redução dos níveis de lipoproteína rica em triglicerídeos e colesterol residual.
Os resultados dos dois estudos de siRNA mostram que esta é uma classe de medicamentos muito promissora que trará novas opções para o tratamento da hiperlipidemia mista e melhorará os resultados cardiovasculares em pacientes.
Horário da postagem: 15 de setembro de 2024