A pneumonia nosocomial é a infecção hospitalar mais comum e grave, sendo a pneumonia associada à ventilação mecânica (PAVM) responsável por 40%. A PAVM causada por patógenos refratários ainda é um problema clínico complexo. Há anos, as diretrizes recomendam uma série de intervenções (como sedação direcionada e elevação da cabeça) para prevenir a PAVM, mas a PAVM ocorre em até 40% dos pacientes com intubação traqueal, resultando em internações hospitalares mais longas, maior uso de antibióticos e morte. As pessoas estão sempre em busca de medidas preventivas mais eficazes.
A pneumonia associada à ventilação mecânica (PAV) é uma pneumonia de início recente que se desenvolve 48 horas após a intubação traqueal e é a infecção nosocomial mais comum e letal na unidade de terapia intensiva (UTI). As Diretrizes da Sociedade Americana de Doenças Infecciosas de 2016 distinguiram a PAV da definição de pneumonia adquirida em hospital (PAH) (PAH refere-se apenas à pneumonia que ocorre após hospitalização sem tubo traqueal e não está relacionada à ventilação mecânica; PAV é a pneumonia após intubação traqueal e ventilação mecânica), e a Sociedade Europeia e a China acreditam que a PAV ainda é um tipo especial de PAH [1-3].
Em pacientes recebendo ventilação mecânica, a incidência de PAV varia de 9% a 27%, a taxa de mortalidade é estimada em 13% e pode levar ao aumento do uso sistêmico de antibióticos, ventilação mecânica prolongada, internação prolongada na UTI e aumento de custos [4-6]. A PAH/PAV em pacientes não imunodeficientes geralmente é causada por infecção bacteriana, e a distribuição de patógenos comuns e suas características de resistência variam com a região, classe hospitalar, população de pacientes e exposição a antibióticos, e mudam ao longo do tempo. Pseudomonas aeruginosa dominou os patógenos relacionados à PAV na Europa e América, enquanto mais Acinetobacter baumannii foram isolados em hospitais terciários na China. Um terço a metade de todas as mortes relacionadas à PAV são causadas diretamente pela infecção, com a taxa de mortalidade de casos causados por Pseudomonas aeruginosa e acinetobacter sendo maior [7,8].
Devido à forte heterogeneidade da PAV, a especificidade diagnóstica de suas manifestações clínicas, exames de imagem e laboratoriais é baixa, e a gama de diagnóstico diferencial é ampla, o que dificulta o diagnóstico atempado da PAV. Ao mesmo tempo, a resistência bacteriana representa um sério desafio ao tratamento da PAV. Estima-se que o risco de desenvolver PAV seja de 3%/dia durante os primeiros 5 dias de uso de ventilação mecânica, 2%/dia entre 5 e 10 dias e 1%/dia durante o resto do tempo. O pico de incidência geralmente ocorre após 7 dias de ventilação, portanto, há uma janela na qual a infecção pode ser prevenida precocemente [9,10]. Muitos estudos analisaram a prevenção da PAV, mas apesar de décadas de pesquisa e tentativas de prevenir a PAV (como evitar a intubação, prevenir a reintubação, reduzir a sedação, elevar a cabeceira da cama em 30° a 45° e cuidados orais), a incidência não parece ter diminuído e a carga médica associada permanece muito alta.
Antibióticos inalatórios têm sido usados para tratar infecções crônicas das vias aéreas desde a década de 1940. Como podem maximizar a entrega de medicamentos ao local alvo da infecção (ou seja, as vias aéreas) e reduzir os efeitos colaterais sistêmicos, eles têm mostrado bom valor de aplicação em uma variedade de doenças. Os antibióticos inalatórios são agora aprovados pela Food and Drug Administration (FDA) dos EUA e pela Agência Europeia de Medicamentos (EMA) para uso em fibrose cística. Os antibióticos inalatórios podem reduzir significativamente a carga bacteriana e a frequência de exacerbações na bronquiectasia sem aumentar os eventos adversos gerais, e as diretrizes atuais os reconheceram como tratamento de primeira linha para pacientes com infecção por Pseudomonas aeruginosa e exacerbações frequentes; Antibióticos inalatórios durante o período perioperatório de transplante de pulmão também podem ser usados como medicamentos adjuvantes ou profiláticos [11,12]. Mas nas diretrizes VAP dos EUA de 2016, os especialistas não tinham confiança na eficácia dos antibióticos inalatórios adjuvantes devido à falta de grandes ensaios clínicos randomizados. O ensaio de Fase 3 (INHALE) publicado em 2020 também não obteve resultados positivos (inalação de antibióticos intravenosos assistidos por amicacina para infecção bacteriana Gram-negativa causada por pacientes com PAV, um ensaio de eficácia de fase 3, duplo-cego, randomizado, controlado por placebos, com um total de 807 pacientes, medicação sistêmica + inalação assistida de amicacina por 10 dias).
Nesse contexto, uma equipe liderada por pesquisadores do Centro Hospitalar Universitário Regional de Tours (CHRU), na França, adotou uma estratégia de pesquisa diferente e conduziu um ensaio clínico randomizado, controlado, multicêntrico, duplo-cego e iniciado pelo pesquisador (AMIKINHAL). Amicacina inalatória ou placebo para prevenção de PAV foi comparada em 19 unidades de terapia intensiva (UTIs) na França [13].
Um total de 847 pacientes adultos com ventilação mecânica invasiva entre 72 e 96 horas foram randomizados 1:1 para inalação de amicacina (N = 417,20 mg/kg de peso corporal ideal, QD) ou inalação de placebo (N = 430, equivalente a 0,9% de cloreto de sódio) por 3 dias. O desfecho primário foi o primeiro episódio de PAV desde o início da randomização até o dia 28.
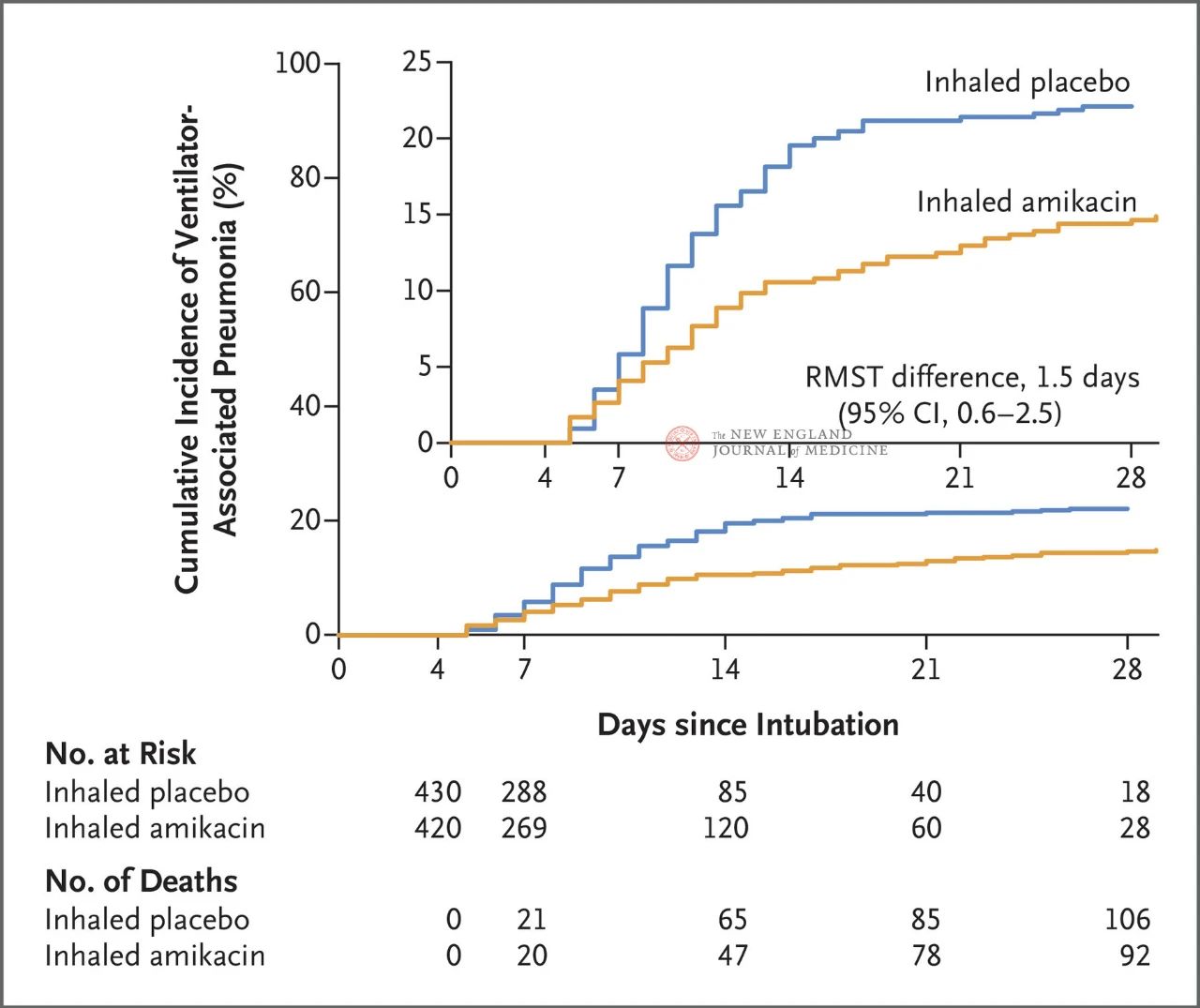
Os resultados do estudo mostraram que, em 28 dias, 62 pacientes (15%) no grupo da amicacina desenvolveram PAV e 95 pacientes (22%) no grupo do placebo desenvolveram PAV (a diferença limitada de sobrevida média para PAV foi de 1,5 dias; IC de 95%, 0,6~2,5; P=0,004).
Em termos de segurança, sete pacientes (1,7%) no grupo amicacina e quatro pacientes (0,9%) no grupo placebo apresentaram eventos adversos graves relacionados ao estudo. Entre aqueles que não apresentaram lesão renal aguda na randomização, 11 pacientes (4%) no grupo amicacina e 24 pacientes (8%) no grupo placebo apresentaram lesão renal aguda no 28º dia (HR, 0,47; IC 95%, 0,23-0,96).
O ensaio clínico teve três destaques. Primeiro, em termos de desenho do estudo, o ensaio AMIKINHAL baseia-se no ensaio IASIS (um ensaio clínico randomizado, duplo-cego, controlado por placebo, de fase 2 paralela, envolvendo 143 pacientes). Para avaliar a segurança e a eficácia do tratamento sistêmico de inalação de amicacina-fosfomicina na infecção bacteriana gram-negativa causada por PAV) e no ensaio INHALE, que terminou com resultados negativos, lições aprendidas, que se concentram na prevenção de PAV, e obtiveram resultados relativamente bons. Devido às características de alta mortalidade e longa permanência hospitalar em pacientes com ventilação mecânica e PAV, se a inalação de amicacina puder alcançar resultados significativamente diferentes na redução de morte e permanência hospitalar nesses pacientes, será mais valiosa para a prática clínica. No entanto, dada a heterogeneidade do tratamento e cuidado tardios em cada paciente e cada centro, há uma série de fatores de confusão que podem interferir no estudo, portanto, também pode ser difícil obter um resultado positivo atribuível a antibióticos inalatórios. Portanto, um estudo clínico bem-sucedido requer não apenas um excelente desenho de estudo, mas também a seleção de desfechos primários apropriados.
Em segundo lugar, embora os antibióticos aminoglicosídeos não sejam recomendados como um único medicamento em várias diretrizes de PAV, os antibióticos aminoglicosídeos podem cobrir patógenos comuns em pacientes com PAV (incluindo Pseudomonas aeruginosa, Acinetobacter, etc.), e devido à sua absorção limitada em células epiteliais pulmonares, alta concentração no local da infecção e baixa toxicidade sistêmica. Os antibióticos aminoglicosídeos são amplamente favorecidos entre os antibióticos inalatórios. Este artigo é consistente com a estimativa abrangente do tamanho do efeito da administração intratraqueal de gentamicina em pequenas amostras publicada anteriormente, que demonstra conjuntamente o efeito dos antibióticos aminoglicosídeos inalatórios na prevenção de PAV. Também deve ser observado que a maioria dos controles placebo selecionados nos ensaios relacionados a antibióticos inalatórios são solução salina normal. No entanto, considerando que a inalação atomizada de solução salina normal em si pode desempenhar um certo papel na diluição do escarro e auxiliar o expectorante, a solução salina normal pode causar certa interferência na análise dos resultados do estudo, o que deve ser considerado de forma abrangente no estudo.
Além disso, a adaptação local da medicação HAP/VAP é importante, assim como a profilaxia antibiótica. Ao mesmo tempo, independentemente do tempo de intubação, a ecologia da UTI local é o fator de risco mais importante para infecção por bactérias multirresistentes. Portanto, o tratamento empírico deve se referir aos dados microbiológicos dos hospitais locais, tanto quanto possível, e não pode se referir cegamente às diretrizes ou à experiência de hospitais terciários. Ao mesmo tempo, pacientes gravemente enfermos que necessitam de ventilação mecânica são frequentemente combinados com doenças multissistêmicas e, sob a ação combinada de múltiplos fatores, como estado de estresse, também pode haver um fenômeno de comunicação cruzada de micróbios intestinais com os pulmões. A alta heterogeneidade de doenças causadas por superposição interna e externa também determina que a promoção clínica em larga escala de cada nova intervenção é um longo caminho a percorrer.
Horário da postagem: 02/12/2023